翻訳|colloid
精選版 日本国語大辞典 「コロイド」の意味・読み・例文・類語
コロイド
改訂新版 世界大百科事典 「コロイド」の意味・わかりやすい解説
コロイド
colloid
均質な媒質中に直径1~500nm(10⁻6~5×10⁻4mm)程度の微粒子あるいは巨大分子が分散している状態(コロイド状態)にある系をコロイドあるいはコロイド分散系という。コロイドとはギリシア語のにかわ(膠)を意味するkollaに由来する名称で,膠質(こうしつ)ともいう。この大きさの粒子(あるいは分子)は普通の光学顕微鏡では見えず,また普通のろ紙を通り,見たところ通常の均一溶液と同じであるが,1粒子当り103~109個の原子を含んでいて,103個以下の原子から成る低分子が分散溶解している溶液とは異なる特徴的な性質を示すことが知られている。コロイドは,大きく粒子コロイド,分子コロイド,会合コロイドの三つに分類することができる。
コロイドの概念と特徴
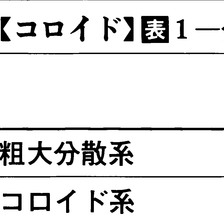
コロイドの概念は1861年イギリスの化学者T.グレアムにより初めて提唱された。彼は種々の物質の拡散の現象を研究し,ある種の物質(硫酸マグネシウム,砂糖など)は速い拡散速度をもつのに対し,別の物質(ゼラチン,アルブミンなど)の移動速度は非常に遅いことを知り,前者がたやすく結晶として取り出すことができるのに対し,後者はそうでないことから,一般に物質は2種に分類できると考え,前者にクリスタロイドcrystalloid,後者にコロイドという名前を与えた。そして半透膜を用いる透析によりクリスタロイドは容易に透析されるのに対し,コロイドは半透膜を通らないことから,両者を容易に分離できることを示した。グレアムの提案は基本的に重要な意味をもつものであったが,この分類は必ずしも適切でないことがすぐに明らかになった。すなわち多くのコロイド,たとえばアルブミンなどのタンパク質は結晶化され,一方ほとんどすべてのクリスタロイドはまたコロイドとすることができることが,実験事実として示された。これによりグレアムのいうコロイドは物質固有の性質を示すものではなく,物質がある大きさの微粒子に分散したときの状態を示すものであることが明らかとなり,F.W.オストワルト(1909)は分散度の概念を導入して分散系を表1のように分類した。このようにしてコロイドの概念は,初めグレアムが提案した物質そのものの分類としてではなく,物質のある分散状態を示すものとして確立されることとなった。
コロイド系が共通してもつ最も重要な性質は,分散粒子が非常に大きな表面積をもつということである。1辺が1cmの立方体は6cm2の表面積をもつが,これをコロイドの典型的な大きさである1辺が10⁻6cmの立方体に分割すると全表面積は6×106cm2に増える。このような微細な粒子が分散しているコロイド系は分散粒子と媒質との広い界面をもち,この界面の物理化学的性質がコロイド系の性質を強く支配する。コロイド系における界面の重要性を初めて指摘したのはドイツのフロイントリヒH.M.F.Freundlich(1907)であり,それ以来コロイドの化学は界面の化学とともに発達した。
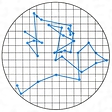
コロイド粒子の構造は1930年ころまでにしだいに明らかにされた。コロイド粒子の存在が初めて実験的に確定したのは,R.シグモンディによる簡単な実験(1900)によってである。彼は金や銀のコロイドに日光を照射し,側方からその光束を顕微鏡で観察したところ,そこに多くの光り輝く粒子が不規則なブラウン運動をしているのを見いだした。これはコロイド系が不均一な分散系であることを直接に証明するものであり,この装置は限外顕微鏡として完成された。A.アインシュタインやM.vonスモルコフスキーのブラウン運動の理論に基づいて,J.B.ペラン(1909)は粗大粒子のブラウン運動の解析から分子の実在性を示したが,同じころT.スベドベリは限外顕微鏡を用いてコロイド粒子のブラウン運動を解析した。彼はその後1924年に超遠心法によるコロイド粒子の大きさの決定法を開発した。
コロイドの種類
金や銀のコロイドなど多くの無機物のコロイドは少量の電解質の添加により凝集し沈殿する。これを凝結という。凝結しやすいコロイドを疎水コロイドhydrophobic colloid,あるいは一般的に疎液コロイドlyophobic colloidという。疎水コロイドは多く微細な結晶質あるいは非晶質の粒子が分散した系で,このように微細ではあるが独立した一つの相をつくる粒子が分散したコロイド系を粒子コロイドという。粒子コロイドが安定に存在する要因は粒子表面の電荷である。
セッケンの溶液がコロイドの一種であることはかなり以前から知られていたが,アメリカのマクベインJ.W.McBain(1913)はこれがセッケン分子の会合によると考え,その会合体をミセルと呼んだ。界面活性剤分子が水溶液中でコロイド次元の会合体を形成することは,その後多くの研究により明らかにされ,これらは会合コロイドと呼ばれる。デンプンやタンパク質など高分子物質は巨大分子からなるので,媒質中に分散して分子コロイドをつくる。これも初めミセル構造をもつ会合コロイドと考えられたが,X線回折などの実験や化学結合理論の発展によって,実は巨大分子であることが,30年ころまでに明らかにされた。巨大分子あるいは高分子の概念はコロイド粒子の構造解明の過程で生まれたともいえるのである。親水性高分子が水中に分散したコロイドは非常に安定で,少量の電解質の添加によって凝結することなく,親水コロイドhydrophile colloid,あるいは一般に親液コロイドlyophilic colloidと呼ばれる。
粒子コロイドparticular colloid
分散コロイドdispersion colloidともいう。粒子コロイドは媒質と粒子の少なくとも二つの相をもち,それぞれの相は気体,液体,固体の場合があるので,表2に示すような種々の型ができる。粒子コロイドをつくるには,大きい粒子を細分してコロイド粒子とする分散法(機械的・電気的・化学的分散,超音波分散),あるいは凝縮法が用いられる。凝縮法としては,溶媒組成を変えたり温度を下げることにより溶解度を下げてコロイド粒子を析出させる方法,あるいは化学反応により生成した物質を成長させる方法がある。コロイドの研究に広く用いられてきた金コロイドは,テトラクロロ金(III)酸HAuCl4水溶液を沸騰させながらホルムアルデヒドで還元することによりつくられる。10~20nmの粒径をもち,ルビー色を示す。
水中に分散した固体粒子は一般に界面に電荷をもっている。系全体としては電気的中性が保たれるので,粒子界面の周辺には粒子電荷と反対符号のイオンがとりまき界面電気二重層をつくる。界面電気二重層のために,電気泳動,電気浸透,流動電位,沈降電位などの界面電気現象を示すが,これらの挙動を支配するのは粒子界面の真電荷ではなく,粒子と媒質の相対運動が生じるすべり面の電位であり,これをゼータ(ζ)電位または界面動電位という。電気二重層をもつ二つの粒子が接近すると,粒子間に働く普遍的な力であるファン・デル・ワールス力のほかに,電気二重層間の相互作用による静電的な反発力が働き,この2種の力のかね合いによって粒子間に働く力がきまる。分散媒の電解質濃度が十分低いときは静電的反発力が勝ち,粒子は凝集せず安定に存在する。電解質濃度が高くなると反発力は小さくなり,粒子は凝集してかたまりとなって沈降する。これが凝結である。凝結に対してはシュルツェH.Schulze(1882)およびハーディW.B.Hardy(1900)によるシュルツェ=ハーディの法則が知られており,それによると凝結は粒子電荷と反対の電荷をもつイオンの価数により強く支配され,2価イオンの凝結力は1価イオンのそれより20~80倍大きく,3価イオンの凝結力は2価イオンのそれより数十倍大きい。これらの疎水コロイドの安定性に対する親水性高分子の添加効果はかなり複雑であり,少量の添加では凝結を促進(増感作用)するが,多量の添加では凝結を抑え安定化(保護作用)する。これは粒子界面への特異的吸着によると考えられ,少量の添加は荷電の部分的遮へいや粒子間の橋架けとして働くが,多量の添加では粒子表面をおおい粒子を親水性とするためである。増感作用を示すものは凝集剤として,保護作用を示すものは保護コロイドprotective colloidとして利用される。古くから保護コロイドとしてアラビアゴム,ゼラチンが有名であったが,最近ではカルボキシメチルセルロース,ポリビニルアルコールなども用いられる。
互いに混じり合わない2液体の一方を他方に分散させ,安定なエマルジョンをつくるためには乳化剤を加える必要がある。乳化剤分子は親水性部分と疎水性部分から成り,2液の界面にあって層状に配列し薄膜をつくる。エマルジョンの安定性はこの薄膜の強さとそれがもつ電荷による。水と油のつくるエマルジョンには二つの型があり,水を連続相とする水中油滴(O/W)型と,油を連続相とする油中水滴(W/O)型である。牛乳は,脂肪滴がタンパク質の薄膜により安定化されたO/W型エマルジョンである。放置すると比重の差により脂肪滴が上部に集まりクリームをつくる。クリームもO/W型の濃厚なエマルジョンである。
分子コロイドmolecular colloid
グリコーゲンやアルブミンなどが水に分散して安定なコロイドをつくることは古くから知られており,とくにこれらは少量の電解質を加えても凝結せず,水に対する親和性の強いことから親水コロイドと呼ばれた。30年ころH.シュタウディンガーらにより巨大分子(高分子)の存在が明らかにされ,巨大分子が単独あるいは少数個集まって浮遊する分子コロイドの概念が確立された。その後多くの高分子物質が合成されるようになったが,伝統的に親水性高分子の水溶液がコロイドとして取り扱われることが多い。分子コロイドには,グリコーゲンやアルブミン,ヘモグロビンのような球形分子コロイドと,デンプン,コラーゲン,フィブリンなどの線形分子コロイドがある。分子の形状は力学的性質に強く反映され,前者が比較的高濃度までニュートン粘性を示すのに対し,後者は低濃度でも非ニュートン性の高粘性を示す。これらの親水性分子コロイドが安定なのは分子表面が強く水和しているためで,多量の電解質を加え水和水を奪うことによって沈殿させることができる。これを塩析という。塩析効果はイオンの水和力の順になり,次の系列が知られている。
陽イオン:Mg2⁺>Ca2⁺>Li⁺>Na⁺>K⁺>NH4⁺
陰イオン:クエン酸イオン3⁻>SO42⁻>Cl⁻
>NO3⁻>Br⁻
これをホフマイスター系列といい,イオンの離液系列と一致する。
分子コロイドとくに線形分子コロイドに特徴的なことはゼリー状になりやすいことである。これは線状分子が長い分子鎖のところどころで会合し系全体にわたる網目構造をつくるためで,その間隙を水分子がうずめる。ゼラチンや寒天がつくるゼリー状構造が典型的であり,非常に軟らかいが固体状態をとりゲルと呼ばれる。しかしこの三次元網目構造をつくる分子鎖の会合はそれほど強くないので,温度が高くなり分子鎖の運動が激しくなるとほどけて液体状態となる。これをゾルという。外力が加わっても分子鎖の結合がほどけてゾルとなり,放置すると再びゲルとなる。このようにゾル-ゲルの変換が可逆的に起こり,かつその変換にかなりの時間がかかると,チキソトロピーなどの複雑な力学的性質を示すようになる。線状高分子を化学的に架橋し網目状高分子とすると,水で膨潤しゲルとなるが,流動性をもつゾルにはならない。
会合コロイドassociation colloid
ミセルコロイドmicelle colloidともいう。親油性の炭化水素基と親水性のカルボキシル基,スルホン酸基,硫酸基,アンモニウム基などをあわせもつ分子は界面活性剤と呼ばれ,その水溶液は低い表面張力をもつ。溶液中である濃度以上になると,数十個の分子が会合しミセルをつくる。この濃度を臨界ミセル濃度critical micelle concentration(略号CMC)という。ミセルはコロイド次元の大きさをもつので,臨界ミセル濃度以上で界面活性剤溶液はコロイド系となり,コロイドに特有の性質を示すようになる。水中で比較的低濃度では疎水性部分を内側に向け親水性部分を外に向けて界面活性剤分子が球状に会合した構造をもつ球形ミセルをつくるが,高濃度になるとさまざまな配向状態をとるようになる。ミセルコロイドは水に溶けない物質を溶解することができる。これはミセルの内部に溶けこむためで,これを可溶化solubilizationという。長鎖アルコールなど極性物質を可溶化させると,これらの分子はミセルの中に配向して入り,ミセルは全体として膨潤して大きくなり,非極性物質をさらに可溶化させるようになる。このような系をマイクロエマルジョンという。非極性溶媒中では界面活性剤分子は極性基を内側に,疎水性基を外に向け会合する。これを逆ミセルという。逆ミセルは水を可溶化することができる。可溶化能の大きい逆ミセルは膨潤してW/O型のマイクロエマルジョンをつくる。界面活性剤のつくるミセルコロイドが会合コロイドの典型的なものであるが,レシチンなど脂質がつくるベシクル(小胞)も会合コロイドの一種であり,生体系では種々の両親媒性物質がつくる会合コロイドが存在し,重要な働きをしていると考えられている。
執筆者:妹尾 学
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
日本大百科全書(ニッポニカ) 「コロイド」の意味・わかりやすい解説
コロイド
ころいど
colloid
ある物質が特定の範囲の大きさ(0.1マイクロメートル程度)の粒子となって他の物質の中に分散している状態をいう。コロイドという名称は、ギリシア語のκολλα(kolla、膠(にかわ))に由来している。そのために日本では以前、膠質(こうしつ)といったことがある。
本来は、食塩や砂糖のような結晶性物質と、ゼラチンやデンプン、タンパク質などのような非結晶性物質を分けるための概念として、イギリスのグレアムが1861年に提唱したものであり、前者をクリスタロイド(晶質)、後者をコロイド(膠質)と名づけたのが始まりである。今日われわれの用いるコロイド関係の用語の多くは、グレアムによって制定されたものが少なくない。しかしその後の研究によって、デンプンやタンパク質も結晶することがわかり、コロイドの性質は、結晶性であるかどうかより、粒子の大きさなどのほうが大きく影響することがわかってきた。
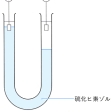
グレアムがこのような分類を行ったのは、水溶液の中における拡散の速度が、食塩やショ糖、塩酸などの水溶液と、膠やデンプン、タンパク質などの水溶液とでは、大きな差があることを発見したからである。この両方を含む水溶液と純水とを、硫酸紙あるいは膀胱(ぼうこう)膜などを隔てて接触させると、コロイドはこの膜を透過できないが、クリスタロイドのほうは純水の方向へ移動・拡散していくので分離できる。これを透析という。しかし、その後コロイド化学の発展につれて、コロイドの概念は拡張され、クリスタロイドのほうは影が薄くなってしまった。
コロイドのなかには、厚さや太さが1~100ナノメートルの膜や繊維までをも含めて取り扱うことが多い。これらはそれぞれに、二次元コロイド、一次元コロイドという。さらに分子自体がナノメートルの桁(けた)の大きさのものになると、このような物質の溶液は、分子溶液であるのにコロイドとしての性質を示すことになる。つまりコロイド分散系である。デンプンやタンパク質、高分子物質の溶液はまさにこのような場合であり、これらを総称して分子コロイドまたは真正コロイドという。
[山崎 昶]
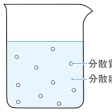
分散質と分散媒
コロイド粒子が分散している(溶解しているとはいわない)液体をコロイド溶液というが、分散している粒子の物質を分散質(分散相ということもある)、分散の媒体を分散媒という。これは溶液における溶質と溶媒に対応している。デンプン溶液などでは、デンプンが分散質、水が分散媒となる。
[山崎 昶]
コロイドの分類
分散質と分散媒の組合せによっては、特定の呼称がつけられているものがある。われわれの身の周りには食品、日用品、家庭用品その他多数のコロイドの実例が存在していることがわかる。また、分散質の集合状態によっても分類できる。
(1)ミセルコロイド(会合コロイド) 界面活性剤、せっけん、染料などのように、溶液の中で分子が数個から数十個会合して生じたミセルがコロイド粒子として分散しているもの。
(2)分子コロイド デンプン、タンパク質などの天然高分子や、ナイロン、塩化ビニルなどの合成高分子は、それだけで(分子1個で)コロイド粒子相当の大きさをもっている。したがって真の溶液のように分子分散をしていても、コロイド溶液としての性質が現れる。
(3)粒子コロイド 水酸化鉄や硫化ヒ素、あるいは金のゾル(カシウスの紫)などのように固体粒子や微結晶がコロイド粒子として分散しているものである。
さらに、分散質と分散媒の親和性によって分類することもしばしば行われている。分散質と分散媒相互に親和性の大のものを親液コロイド、小のものを疎液コロイドという。水と油に対して、それぞれ親水コロイド、疎水コロイド、親油コロイド、疎油コロイドが存在する。
(1)親水コロイド 水を分散媒とするゾル(ヒドロゾル)のうちで、分散質が水との親和性に富むものをいう。デンプン、アルブミンなどの高分子電解質、あるいは界面活性剤からなるミセルなどはこの親水コロイドに区分される。少量の電解質を加えても簡単には凝結をおこさないが、アルコールとか、かなり大量の電解質を加えると凝結がおこる(たとえば豆腐など)。チンダル現象も疎水コロイドに比べて見えにくく、限外顕微鏡によっても粒子が認めがたいものが多い。表面張力は概して水より小、粘性率は水より大の傾向がある。
(2)疎水コロイド 水を分散媒とするコロイドのうち、ごく少量の電解質を加えるだけで容易に凝集、沈殿を生じるもの。一般に強いチンダル現象を示す。金属粒子や金属の硫化物などの無機物のコロイドの多くはこの疎水コロイドである。限外顕微鏡で容易に粒子を観察できる。
[山崎 昶]
コロイド溶液の性質
コロイド分散系に光束を当てて側面から見ると、光の通路が鮮やかに光って見える。これをチンダル現象またはチンダル効果という。コロイド粒子による光の散乱である。コロイド粒子はそのままでは顕微鏡で見ることはできないが、限外顕微鏡によって粒子のブラウン運動を観察することができる。コロイド粒子は一般に電荷を保持していて、電極を入れて直流電圧を加えると、それぞれの電荷に応じて反対側の電極のほうへ移動する(電気泳動)。コロイド粒子は同符号の電荷をもっているために、互いに反発しているから溶液中に安定に分散しているのだが、これと反対符号の電荷をもつイオンを加えると、コロイド粒子間の反発力よりも引力がまさって凝集が始まり、ときには沈殿を生じる。これを凝析(凝結)という。凝析能力は多価のイオンほど大であり、豆腐をつくる際に塩化マグネシウムや硫酸カルシウムを加えるのは、これらが1価のイオンよりずっと低濃度でも有効に凝析をおこすことを利用している。廃水処理などで硫酸アルミニウムやミョウバンなどを添加するのも、アルミニウムイオンによる凝析の利用である。
高分子の電解質を加えた際におこる凝析は、イオンの価数が大きいためにずっと顕著である。ベントナイトの懸濁液にドジョウを放すと、表皮から分泌される粘液の中の高分子電解質のために凝析がおこり水は清澄になる。この原理を定量分析に応用したのがコロイド滴定である。東京大学の寺山宏(てらやまひろし)により1948年(昭和23)に創案されたが、当初は好適な試薬が得がたかったこともあり、なかなか正当な評価を得られなかったが、近年、世界的に普及した便利な方法となった。
コロイド溶液において、疎水コロイドが凝結するのを防ぐために親水コロイドを加えることがある。このようにすると分散系は安定になるが、この際に加える親水コロイドを保護コロイドという。
[山崎 昶]
コロイド溶液のつくり方
巨大分子の溶液、すなわち分子コロイド溶液をつくるには、適当な溶媒を選んでゆっくり温めることにより簡単に可能となる。デンプンやゼラチン、寒天など台所で実際につくっている例には事欠かない。疎液コロイドやミセルコロイドをつくるには、これよりも多少むずかしい。ミセルコロイドは、界面活性剤、せっけんなどを臨界ミセル濃度(CMC)以上となるように注意して溶液をつくると生じる。金属のコロイドは、水中で放電により微粒子をつくらせたり、超音波で分散させたりして物理的に調整する方法と、化学的に還元によって微粒子をつくらせる方法がある。前にもあげた金のコロイドであるカシウスの紫は、塩化スズ(Ⅱ)による還元を利用している。硫化水銀や水酸化アルミニウムなどは超音波分散法で調製できる。
また、濾紙(ろし)上に集めた沈殿を熱水で洗うと、解膠(かいこう)(ペプチゼーション)によってコロイド溶液がつくられる。水酸化鉄(Ⅲ)のコロイドはよくこの方法でつくられるが、重量分析などに際しては解膠がおきないように、硝酸アンモニウムなどの電解質を溶かした洗液で沈殿を洗うことになっている。水酸化鉄のコロイドは、塩化鉄(Ⅲ)の濃厚溶液を熱水で希釈しても得られるし、希薄水溶液を加熱してもよい。温泉場などで売っている「湯の華(はな)」は硫化水素の酸化によって生じた硫黄(いおう)のコロイドを集めて固めたものである。浴用、薬用、化粧品として用いられる。
いずれにせよコロイド溶液には多かれ少なかれ種々の不純物が混入してくる。粒の大きいものは濾紙で濾過して除けるが、イオン性の不純物を除くには、前にも述べた透析による。セロファン膜などの袋にコロイド溶液を入れて、袋の外側を新しい分散媒(水など)で洗うと、低分子のものは膜を透過するが、コロイド粒子は膜の内側に残るので精製できる。外側に直流電圧をかけて電場によるイオンの移動を利用すると、ずっと迅速に透析ができる。もっとも、コロイドによっては、あまり精製すると粒子上の電荷まで外れてしまい不安定となるものもあるので注意が必要である。
[山崎 昶]
『近藤保・鈴木四朗著『やさしいコロイドと界面の科学』(1983・三共出版)』▽『中垣正幸・福田清成著『コロイド化学の基礎』(1968・大日本図書)』
百科事典マイペディア 「コロイド」の意味・わかりやすい解説
コロイド
→関連項目暗視野顕微鏡|限外ろ(濾)過|サイズ|シグモンディ|シュリーレン法|晶質|粘弾性|分散染料
出典 株式会社平凡社百科事典マイペディアについて 情報
岩石学辞典 「コロイド」の解説
コロイド
| 系 | 粗粒 | コロイド分子 | |
|---|---|---|---|
| (分散物+媒質) | |||
| 固体+固体 | 鉱物の固溶体 | 青色の岩塩(NaCl中のNa) | 固溶体 |
| 固体+液体 | 懸濁液(suspention) | suspensoid | 溶液 |
| 固体+気体 | 塵,火山灰 | 煙 | |
| 液相+液体 | 乳濁液(emulsion) | emulsoid | 溶液 |
| 液相+気体 | 雨 | 霧 | |
| 気体+固体 | 気体の包有物 | 吸蔵された気体 | 吸収された気体 |
| 気体+液体 | 泡 | コロイド泡 | 溶液 |
| 気体+気体 | 溶液 |
化学辞典 第2版 「コロイド」の解説
コロイド
コロイド
colloid
1861年,T. Graham(グラハム)は水のなかで,にかわ,デンプン,タンパク質などの水溶液が拡散する速度が,塩酸,食塩,硫酸マグネシウム,ショ糖(スクロース)の水溶液に比べて格段に遅いことを発見し,前者をコロイド(こう質),後者をクリスタロイド(晶質)と名づけた.また,上記2種類の溶液の混合液と水とを動物膜あるいは硫酸紙で仕切ると,クリスタロイドは膜を通過して水のほうに移るが,コロイドのほうは膜を通りにくく,この方法で両者を分離することができることを示した.これを透析という.その後,C.W.W. Ostwald(オストワルト)は分散状態論の立場から,あらゆる物質の径が 10-5~10-7 cm 程度に分散された状態が,Grahamのいうコロイド状態に相当することを指摘して以来(1907年),コロイドの概念は気相を分散媒とする霧や煙,固相を分散媒とする着色ガラスなどにも拡張されるとともに,厚さや太さが 10-5~10-7 cm 程度の膜や繊維にまで拡張され,それぞれ二次元的および一次元的コロイドと考えられるようになった.また,分子の大きさが上記の大きさに相当する場合には,その溶液は分子溶液であるとともにコロイド分散系に属することになる.これを真正コロイド(eukolloid)あるいは分子コロイドという.いわゆる高分子の溶液は分子コロイドである.Grahamが最初に示したコロイドは,いまから見るといずれも天然高分子にほかならない.コロイド分散状態を得るためには,低分子の集合による凝集法と,大きいものを分割破砕してコロイドを得る分散法とがある.[別用語参照]分散系
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
ブリタニカ国際大百科事典 小項目事典 「コロイド」の意味・わかりやすい解説
コロイド
colloid
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
最新 地学事典 「コロイド」の解説
コロイド
colloid
分散した微粒子が別の物質中に浮遊している混合物。漢字では膠漆
執筆者:木村 勇気
出典 平凡社「最新 地学事典」最新 地学事典について 情報
栄養・生化学辞典 「コロイド」の解説
コロイド
世界大百科事典(旧版)内のコロイドの言及
【グレアム】より
…33年にはリン酸の研究によって多価の無機酸(多塩基酸)の概念を提唱して,J.vonリービヒに影響を与えた。また液体の拡散を研究して非拡散物質を〈コロイド〉と命名,透析法を考案して〈コロイド〉と〈クリスタロイド〉を分離し,コロイド化学への道を開いた。彼の教科書《化学要綱Elements of Chemistry》(1841)は広くヨーロッパ全域で読まれた。…
※「コロイド」について言及している用語解説の一部を掲載しています。
出典|株式会社平凡社「世界大百科事典(旧版)」
関連語をあわせて調べる
半夏ともいう。七十二候の一つで,本来は夏至後 10日目から小暑の前日までをいったが,現行暦では太陽の黄経が 100°に達する日 (7月1日か2日) を半夏生とし,雑節の一つとして記載している。この頃半...