翻訳|ion
共同通信ニュース用語解説 「イオン」の解説
イオン
グループ年間売上高が6兆円を超え、セブン&アイ・ホールディングスと並ぶ流通大手。郊外型の大型スーパーに加え、都市圏を強化する戦略を打ち出している。5月にはイオン子会社マックスバリュ関東と、マルエツ、カスミを統合して、首都圏スーパー連合をつくる計画を発表した。2007年にダイエー、丸紅と資本・業務提携を結び、13年にダイエーを連結子会社化した。ダイエーの不振などが響き、14年3~5月期連結純利益は前年同期比90・1%減の13億円。
更新日:
出典 共同通信社 共同通信ニュース用語解説共同通信ニュース用語解説について 情報
精選版 日本国語大辞典 「イオン」の意味・読み・例文・類語
イオン
- 〘 名詞 〙 ( [ドイツ語] Ion・[英語] ion ) 正または負に荷電した原子や原子団。電気的に中性の原子や分子が電子を失い、または得ることによってその電子の数だけの電気量(イオン価)を帯び、それぞれ陽イオン、陰イオンとなる。電解質を溶媒にとかすと陰陽両イオンに、気体分子を放射線やX線等で照射すると陽イオンとなる。気体放電などによっても陽イオンが発生する。〔物理学術語和英仏独対訳字書(1888)〕
日本大百科全書(ニッポニカ) 「イオン」の意味・わかりやすい解説
イオン(原子)
いおん
ion
原子あるいは原子団において、それを構成する全原子核のもつ正電荷数と、全電子(電子の記号はe-)のもつ負電荷数とが同じでないものをイオンという。
[岩本振武]
イオンの発見
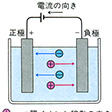
電解質、たとえば塩化ナトリウムNaClの水溶液に直流電流を通じると、低電位極(負極、陰極cathode)へ向かってナトリウムの原子が移動し、高電位極(正極、陽極anode)に向かって塩素の原子が移動する。この現象をイギリスのファラデーは、ナトリウムの原子が正の電荷をもち、塩素の原子が負の電荷をもっているためと説明し、これらの電荷をもつ原子を「移動する」という意味のギリシア語ionaiからイオンionと命名した。その後、電子の存在や原子の電子構造などの研究が進み、イオンとは中性原子あるいは原子団における整数個の電子の得失によって生ずるものであることが明らかにされた。
[岩本振武]
陽イオンと陰イオン
正電荷数が過剰のもの、すなわち中性の原子または原子団から電子が失われたものを陽イオン(カチオンcation)といい、負電荷数が過剰のもの、すなわち中性の原子または原子団に電子が加わったものを陰イオン(アニオンanion)という。陽イオンは正イオン、陰イオンは負イオンとよぶこともある。
[岩本振武]
両性イオン
中性の分子であっても、陽イオン部分と陰イオン部分を含む構造をもつものがあり、これを両性イオンという。アミノ酸はその分子中にアミノ基-NH2とカルボキシ基-COOHとをもつが、水溶液中や結晶中で両性イオンとなりやすいことが知られている。
NH2-R-COOH→NH3+-R-COO-
[岩本振武]
イオン記号、イオン価
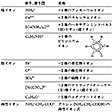
イオンは、そのもととなる原子あるいは原子団の化学記号の右肩に、得失した電子の個数を符号とともに示した記号であるイオン記号で表される。得失した電子の個数はイオン価であり、一般に正n価の陽イオンはMn+とし、負n価の陰イオンをXn-のように示す。n+のかわりに+nを、n-のかわりに-nを用いたり、+や-を価数だけ列記すること(Fe+++、SO4--)もあるが、現在では正式の表記法ではない。イオン1個のもつ電気量は電子1個のもつ電気量の絶対値(電気素量)のイオン価倍になる。
[岩本振武]
イオン化
原子、分子、あるいは原子団が1個以上の電子を失うか、得るかしてイオンになることをイオン化または電離という。陽イオン化に必要なエネルギーをイオン化エネルギー、陰イオン化に際して放出されるエネルギーを電子親和力という。
γ(ガンマ)線、X線、紫外線などの高エネルギー電磁波や、電子を高電圧で加速した電子線を照射したり、高温度に加熱して熱エネルギーを供給すると、原子や分子がイオン化される。地球の高層大気には、太陽からの紫外線、X線および宇宙線によって生ずると考えられるイオン層(電離層)が数層あって、その電荷密度や層構造は昼夜間、日食などによる太陽の影響を大きく受けている。ガイガー‐ミュラー計数管や霧箱(きりばこ)は、放射線によるイオン化を利用した気体電離型の放射能測定装置である。
化学反応によるイオン化は酸化還元反応であり、たとえば2種の単体が反応する際、一方が陽イオン化すれば他方は陰イオン化し、陽イオン化する物質から陰イオン化する物質へ電子が移動する。
[岩本振武]
溶液中のイオン
水その他の電離性溶媒に溶けて陰・陽両イオンを与える物質を電解質という。電離性溶媒の分子は一般に極性分子であり、それ自身電離平衡によって陽イオンと陰イオンに解離する。
水やアンモニアのように電離の際に水素イオン(プロトン。重水素イオンも含めた厳密な表記では、ヒドロン)の移動を伴う溶媒はプロトン性溶媒であり、二酸化硫黄のようにプロトンを含まない溶媒は非プロトン性溶媒である。これらの溶媒の電離平衡定数は一般にきわめて小さく、水の場合でも25℃で
[H3O+][OH-]=10-14mol2dm-6
程度である。
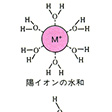
電解質が水に溶けると、陽イオンの周りには電気的に負な酸素原子が配向して水分子が集まり、水和構造をつくる。陰イオンの周りには電気的に正の水素原子が配向して水分子が引き付けられる。陽イオンと陰イオンが静電引力で凝集したイオン結晶が水に溶けるのは、結晶を形成しているよりも、各イオンが水和構造をつくって分散するほうがエネルギー的に安定になるからである。もし水和したほうが不安定になるならば、その結晶は水に溶けにくくなる。
電解質はかならずしもイオン結晶だけとは限らず、たとえば塩化水素HClは共有結合性分子であるが、水に溶けると電離して塩酸となる。
HCl+H2O→H3O++Cl-
塩酸中にはHCl分子はほとんど存在せず、電離はほぼ100%進行する。このような物質は強電解質であり、電離度の小さい物質は弱電解質である。
電解質が水に溶けたときに水分子と化学反応をおこすことがある。酸化物イオンO2-は固体中や融解塩中には存在するが、水に溶けると水酸化物イオンになる。
O2-+H2O→2OH-
水素イオンH+も単独には存在せず、一般にH(H2O)n+として数個の水分子と水和した状態になっている。これをオキソニウムイオンといい、nは4以上と考えられているが、一般にはH3O+の記号で表している。
陽イオンは、中性原子から電子が失われたものであるから、残っている電子はますます強く原子核に引き付けられ、イオン半径が小さくなって正の電荷密度も大きくなる。そのため、水分子の酸素原子は多価陽イオンに強く引き付けられ、水分子内の電子も酸素原子側に移動して、水素原子はより陽イオン的となる。その結果、水素原子は陽イオンとなって放出され、多価陽イオン全体の正電荷を見かけ上減少させようとする。これは加水分解の一種であり、Al3+、Fe3+、Ti4+、V5+などの陽イオンはとくに加水分解を受けやすい。チタン(Ⅳ)やバナジウム(Ⅴ)などの陽イオンは単独では水溶液中に存在できず、オキシドチタン(Ⅳ)イオン(チタニルイオン)TiO2+やジオキシドバナジウム(Ⅴ)イオン(バナジルイオン)VO2+などのオキソイオンとなる。クロム(Ⅵ)やマンガン(Ⅶ)などのように大きなイオン価をもつイオンになると、陽イオンとしてではなく、クロム酸イオンCrO42-や過マンガン酸イオンMnO4-などのような陰イオン、オキソ酸イオンになって存在している。
水和水は溶媒の水と絶えず交換されているが、その交換速度は陽イオンの電荷密度が高くなるにつれて遅くなる。強く水和した陽イオンは、水分子を配位子とする錯イオンと考えられる。d軌道電子が9個以下の遷移元素のイオンが水溶液中で示す特有の色は、水を配位子とする錯イオンの色である。銅(Ⅱ)の硝酸塩や硫酸塩の水溶液は青色を呈するが、これはテトラアクア銅(Ⅱ)イオン[Cu(H2O)4]2+の色である。水よりも強い配位能力をもつ配位子を加えると、配位水和水との置換がおきて新しい錯イオンが生成する。たとえば、銅(Ⅱ)塩の水溶液にアンモニア水を加えると、テトラアンミン銅(Ⅱ)イオン[Cu(NH3)4]2+が生じて、溶液は青紫色となる。
[岩本振武]
多原子イオンの構造
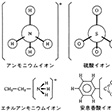
アンモニア分子に水素イオンが付加するとアンモニウムイオンを生ずる。
NH3+H+→NH4+
しかしその構造はメタンCH4と同じ正四面体型となり、4個の水素原子の中のどれがH+であるかの区別はできない。NH4原子団が全体として+1価の陽イオンになっているのである。同様に硫酸H2SO4(=SO2(OH)2)から生ずる硫酸イオンSO42-においても、その構造は正四面体型であり、4個の酸素原子は等価である。一方、アルキルアミンやカルボン酸のような有機電解質では、それぞれの官能基だけがイオン化していると考えたほうがよく、分子全体に均等な電荷分布があるわけではない。
[岩本振武]
『ロナルド・W・ガーネイ著、鈴木伸訳『イオン溶液論』(1966・産業図書)』
イオン(株)
いおん
イオングループを統轄する純粋持株会社。1758年(宝暦8)に三重県四日市(よっかいち)で開業した太物・小間物商篠原屋(1887年岡田屋と改称)が源流。1926年(大正15)に株式会社岡田屋呉服店となり、第二次世界大戦後の1959年(昭和34)に岡田屋に社名変更した。1969年に、いずれもチェーン展開していた岡田屋、フタギ、シロの3社が共同仕入機構としてジャスコを設立、また東北地方の有力チェーン6社の提携で、東北ジャスコグループを結成した。1970年には岡田屋がフタギ、オカダヤチェーン、カワムラ、共同仕入機構ジャスコを合併し、ジャスコに社名変更した。「ジャスコ」の名はJapan United Stores Companyを略したJUSCOからきている。その後も1970年代には地方のローカル・チェーンとの提携・合併を繰り返して、大規模なナショナル・チェーンを構築し、いわゆる「連邦経営」を展開していった。1980年代にはコンビニエンス・ストアのミニストップ、外食産業のレッドロブスター、自動車販売のオートラマライフなど、新業種や新業態に活発に進出した。アメリカの婦人服専門店チェーンのタルボット社の買収など海外進出も図り、グループ名も新たにイオングループとし、2001年(平成13)8月には社名・グループ名もともにイオンと変更した(ジャスコの名はしばらく店名として継続していたが、順次イオンに変更された)。2003年に、会社更生法の適用を受けていた大手スーパーのマイカルとその関係会社を傘下に加える。さらに2005年フランスの大手小売企業カルフールの日本法人、カルフール・ジャパンを完全子会社化し、社名をイオンマルシェに変更した。2007年10月、イオン銀行の営業を開始。流通業からの銀行業参入はセブン銀行に次いで2番目となる。2008年8月純粋持株会社へ移行し、小売事業等はイオンリテールに承継した。2013年8月には大手小売企業ダイエーをTOB(株式公開買付)により連結子会社化、2015年1月に株式交換により完全子会社化した。資本金2200億0700万円(2015)、売上高7兆0785億円(2015年2月。連結ベース)。
[中村青志]
『ジャスコ株式会社編・刊『ジャスコ三十年史』(2000)』
イオン(ギリシアの伝説)
いおん
Iōn
ギリシアの伝説で、イオニア人に名を与えたとされる人物。アテネ王エレクテウスの娘クレウサは、アポロン神に誘惑されてイオンを生むが、処置に困ってこれを捨て、クストスと結婚する。クストスは、舅(しゅうと)エレクテウスの死後アテネ王となるが、夫婦は子宝に恵まれないため、子が授かるように神託を求めてデルフォイに赴く。神託は、神殿を出て最初に出会う者をわが子とせよというものであったが、その者こそアポロンの計らいで無事成長したイオンであった。ところがクレウサは彼をクストスの隠し子と誤解し、老僕の協力を得てこれを毒殺しようとするが露見し、逆に窮地に陥る。だがここで巫女(みこ)ピティアが介入し、母子の再認が成立して大団円となり、ともにアテネへ戻ってイオンはイオニア人の祖となる。
以上はエウリピデスの劇によって知られている伝承であるが、イオンをクストスの実子とする異伝もあり、そこでもイオンは、紆余(うよ)曲折ののちアテネ王となり、イオニア人の祖となっている。
[丹下和彦]
改訂新版 世界大百科事典 「イオン」の意味・わかりやすい解説
イオン
ion
中性の原子または原子団が1個または数個の電子を失うか,あるいは1個または数個の電子を得て生ずる粒子をいう。たとえばナトリウムイオンNa⁺,塩化物イオンCl⁻,塩素酸イオンClO3⁻などがそれである。ある種の物質(固体電解質)を加熱して融解し,その電気抵抗を測定してみると,その融解液の電気抵抗は小さく,すなわち電気を通す性質をもっていることがわかる。さらにこの種の物質について,その構成要素を調べてみると,その最小単位の大きさは,原子や分子の大きさと同程度(1オングストロームÅ=10⁻10m程度)であるが,電気的に中性の原子や分子とは異なり,正または負の電荷をもっていることがわかる。歴史的にさかのぼれば,電解質溶液に電流を流して電気分解を行うときに,アノードanode(陽極)へ向かって行く粒子とカソードcathode(陰極)へ向かって行く粒子があることから,M.ファラデーが〈行く〉という意味のギリシア語にちなみ,その粒子をイオンと名づけ,そしてカソードへ向かう粒子をカチオンcation(陽イオン),アノードへ向かう粒子をアニオンanion(陰イオン)と呼んだ。イオンの帯電の原因が1個または数個の電子の授受によることからわかるように,イオンがもつ電荷の量は電気素量e(=1.6021892×10⁻19C)の整数(正または負)倍に等しい。この整数の値をイオン価valency,イオンの価数,イオンの電価などといい,イオンを表すさいには,このイオン価と電荷の符号を化学式の右肩に付してH⁺,Ca2⁺(またはCa⁺⁺),SO42⁻(またはSO4⁻⁻)などのように書く。H⁺は1価の陽イオン,Ca2⁺は2価の陽イオン,SO42⁻は2価の陰イオンである。
イオンは,電解質の溶解液(溶融塩)や溶液の中で生成するばかりでなく,気体放電や気体の放射線照射,分子の中での電子移動などによっても生成する。このようなイオン生成現象をイオン化あるいは電離という。とくに解離あるいは放射線によってイオンが生じる場合は電離と呼ぶのがふつうである。
水溶液中のイオン
ふつうの状態(常温,常圧)でイオンが存在しやすいのは,水溶液のような極性液体中においてである。気体では高温,低圧の状態でのみ,ある程度のイオンが存在しうるにすぎない。また溶融塩も,高温にして融解状態を保つことによって初めてイオンの特性(たとえば電気分解など)が確かめられる。水溶液中においてイオンが容易に存在しうるのは,イオンと溶媒である水との相互作用,すなわち水和と呼ばれる溶媒和現象による。イオンは帯電しているために,異符号のイオンどうしが強く引き合い,また同符号のイオンどうしは強く反発し合うはずである。ところが水溶液中では,水和のためにイオン間の静電的な相互作用が弱められており,イオンとして存在しやすくなっているのである。
→イオン化エネルギー →イオン化傾向
執筆者:橋谷 卓成
出典 株式会社平凡社「改訂新版 世界大百科事典」改訂新版 世界大百科事典について 情報
ブリタニカ国際大百科事典 小項目事典 「イオン」の意味・わかりやすい解説
イオン
イオン
ion
イオン
Iōn
イオン
Iōn
イオン[キオス]
Iōn of Chios
[没]?
ギリシアの悲劇詩人,抒情詩人。悲劇作品は現存しないが,ソフォクレスの温和で洗練された人柄を論評した文章の一部が伝わっている。
出典 ブリタニカ国際大百科事典 小項目事典ブリタニカ国際大百科事典 小項目事典について 情報
百科事典マイペディア 「イオン」の意味・わかりやすい解説
イオン
→関連項目陰イオン|モル|陽イオン
イオン[株]【イオン】
→関連項目カルフール[会社]|ミニストップ[株]|ヤオハンジャパン[株]
出典 株式会社平凡社百科事典マイペディアについて 情報
知恵蔵 「イオン」の解説
イオン
(市村禎二郎 東京工業大学教授 / 2007年)
出典 (株)朝日新聞出版発行「知恵蔵」知恵蔵について 情報
化学辞典 第2版 「イオン」の解説
イオン
イオン
ion
荷電した原子または原子団をイオンといい,正または負に帯電したものをそれぞれ陽イオン(あるいはカチオン),陰イオン(あるいはアニオン)という.M. Faraday(ファラデー)が電解質溶液を用いて電解を行ったとき,溶液中に電場の存在下で電極に向かって移動するものがあることを見いだし,ギリシア語の“行く”という意味にちなんでイオンと名づけた.また,電解質溶液の場合に限らず,気体分子が電子を失ったり,得たりして,正負の電気を帯びた場合も,それをイオンという.中性の原子あるいは分子がイオンになることをイオン化または電離という.イオンのもつ電気量は電気素量の整数倍に等しく,この倍数がイオン価である.イオンを表示するには,一価の陽イオンならば原子記号の肩に+,一価の陰イオンならば-をつけ,二価以上のときには Cu2+,Fe3+,PO43-などのように表す.
出典 森北出版「化学辞典(第2版)」化学辞典 第2版について 情報
日本の企業がわかる事典2014-2015 「イオン」の解説
イオン
デジタル大辞泉プラス 「イオン」の解説
イオン
栄養・生化学辞典 「イオン」の解説
イオン
関連語をあわせて調べる
ローマ法王ともいう。ラテン語 Papaの称号はカトリック教会首長としてのローマ司教 (教皇) 以外の司教らにも適用されていたが,1073年以後教皇専用となった。使徒ペテロの後継者としてキリスト自身の定...